در این پست برای شما کاربران عزیز انیمیشن دوبله فارسی فوتبال دستی ( Metegol ) رو گذاشتیم که محصول سال 2014 است و واقعا هیجان انگیزه.شما می توانید این انیمیشن فوق العاده را به صورت کاملا رایگان از T.KDOWNLOAD دانلود کنید و لذت ببرید.نظر یادتون نره!


در این پست برای شما کاربران عزیز انیمیشن دوبله فارسی فوتبال دستی ( Metegol ) رو گذاشتیم که محصول سال 2014 است و واقعا هیجان انگیزه.شما می توانید این انیمیشن فوق العاده را به صورت کاملا رایگان از T.KDOWNLOAD دانلود کنید و لذت ببرید.نظر یادتون نره!

فعل امر:فعلی است که بر دستور وفرمان به انجام یک کار دلالت می کند.
براى ساخت فعل امر می بایست از صیغهی مضارع مخاطب استفاده نماییم.
مراحل:
1)حرف مضارعه(ت) حذف مى شود.
2) آخر فعل مجزوم مى شود یعنی اگر آخر فعل ضمه داشت، ضمه تبدیل به ساکن میشود و اگر آخر فعل نون داشت،نونِ آخر حذف میشود ،البته بجز نون ِجمع مؤنث که باقی میماند وحذف نمیشود.
3)حالا اگر بعد از حذف (ت) ، اولِ فعل ساکن باشد،یک همزه به اول آن اضافه میکنیم.که حرکت همزه کسره میباشد مگر اینکه حرکت عین الفعل (ضمه) باشد که در این صورت حرکت همزه نیز ضمه خواهد بود.
مثـــــــال: تَکتُبینَ فعل امرش میشود: اُکْتُبی
تَذْهَبُ میشود: إذْهَبْ / تَذْهَبْنَ می شود: إذْهَبْنَ
*در جدول زیر شیوه ساخت فعل امر از صیغه مضارع مخاطب آمده است:
|
مــــــذکـــــــــر |
مــــــــــؤنــــث |
|
مخاطب / امـــــــر |
مخاطب / امــــــــر |
|
تَذْهَبُ إذْهَبْ (برو) |
تَذْهَبینَ إذْهَبی (برو) |
|
تَذْهَبانِ إذْهَبا (شما دونفربروید) |
تَذْهَبانِ إذْهَبا (شما دونفر بروید) |
|
تَذْهَبونَ إذْهَبوا (شما چند نفر بروید) |
تَذْهَبْنَ إذْهَبْنَ(شما چند نفر بروید) |
نکتــــــــه- اما اگر بعد از حذف (ت)،اول فعل ساکن نبود ،همزه به اول فعل اضافه نمیشود.(یعنی باید قابل خواندن باشد.)
مثـــــــال: تُجاهِدونَ فعل امرش میشود: جاهِدوا
تُعَیِّنُ میشود : عَیِّنْ / یُبَلِّغُ میشود: بَلِّغْ
هرگاه بخواهیم دو صیغه ی غائب ومتکلم مضارع را به انجام کارى که با وجوب و باید همراه است ،فرمان دهیم ،چون که مخاطب ما نیستند تا مستقیما آنها را به انجام کار فرمان دهیم،از شیوه ای دیگر استفاده میکنیم.
برای ساخت این فعل، حرف (لِ ) قبل از فعل می آید وآخر آن مجزوم میشود.(مجزوم کردن یعنی تبدیل ضمه به ساکن و وحذف نون آخر ،بجز نون جمع مؤنث)
مثـــــــال: یَذْهَبُ :لِیَذْهَبْ (باید برود) / یَجْلِسونَ : لِیَجْلِسوا (باید بنشینند) /نذْهَبُ : لِنَذْهَبْ (باید برویم)
دانلود سوالات امتحان قرآن - ماهانه مهر ماه
|
سوالات امتحان قرآن - ماهانه مهرماه 1393 |
|
|
فرمت فایل |
|
|
حجم فایل |
310 KB |
|
تهیهکننده |
زارعی |
مثلث خیام - پاسكال

نحوه رسم9 ضلعی منتظم

نحوه رسم6 ضلعی منتظم

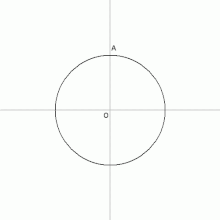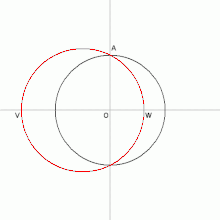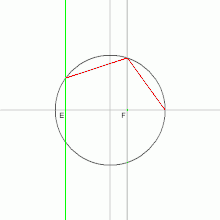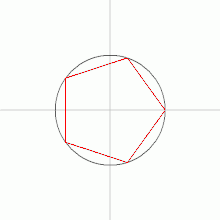
نحوه رسم5 ضلعی منتظم
نحوه رسم4 ضلعی منتظم

شش اتحاد کارآمد
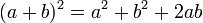


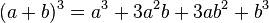
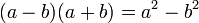


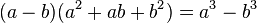
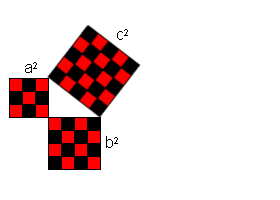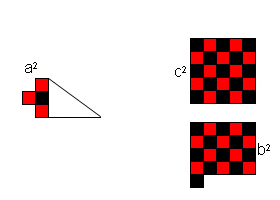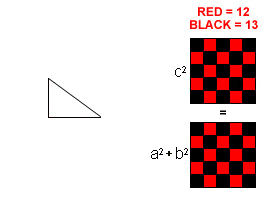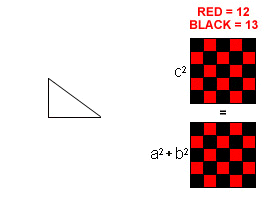
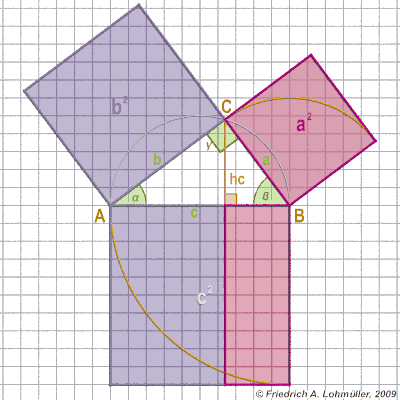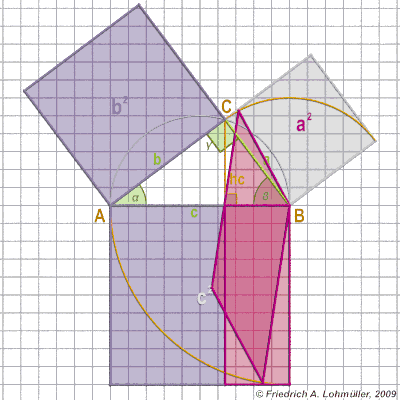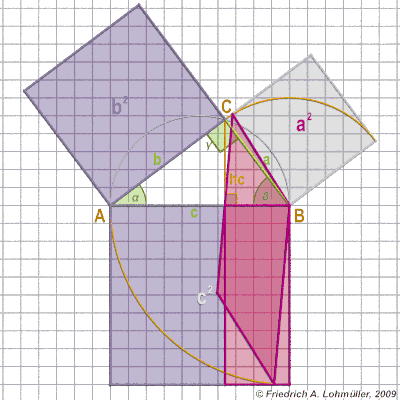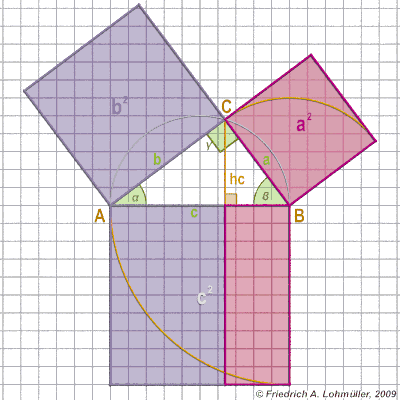
*******رابطهی فیثاغورس (ص 84)************
******** منبع: Riazi7.ir *** *******
************** *************************************
چند انیمیشن برای اثبات قضیه فیثاغورس
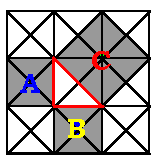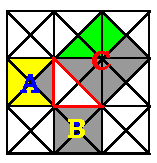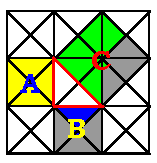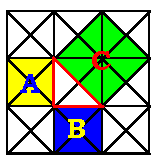
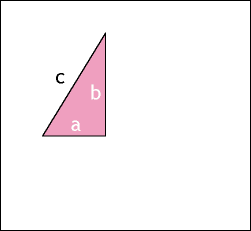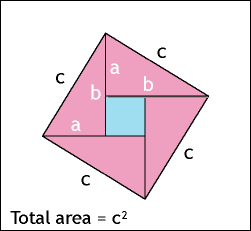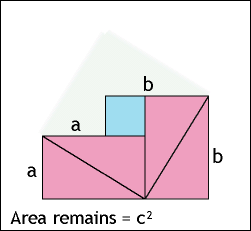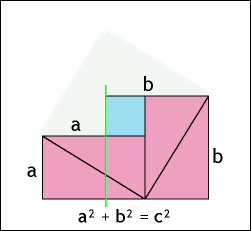
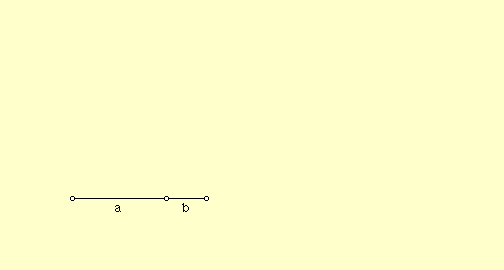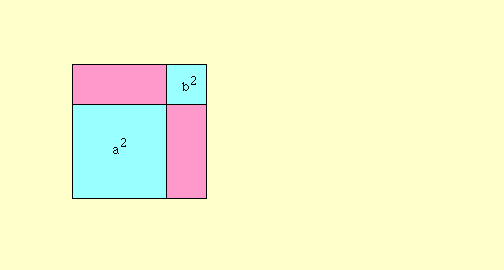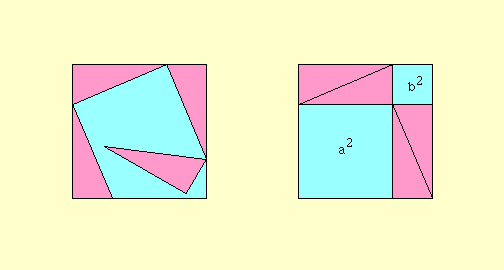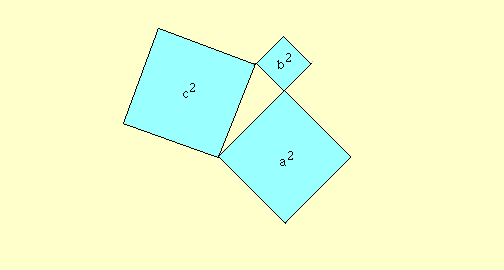
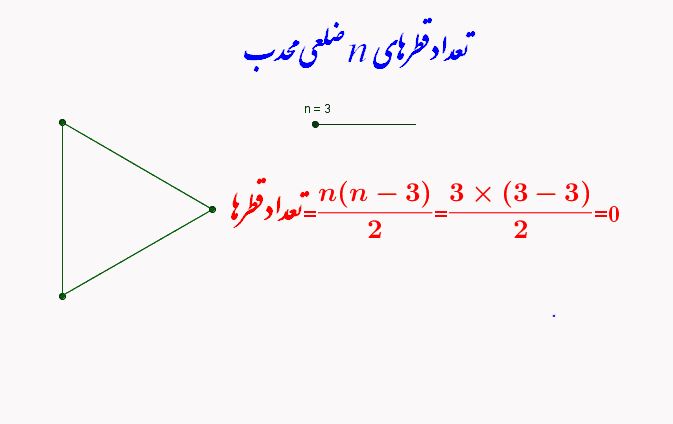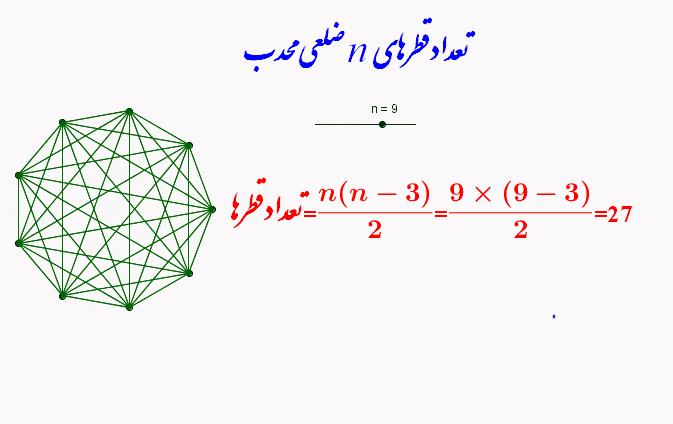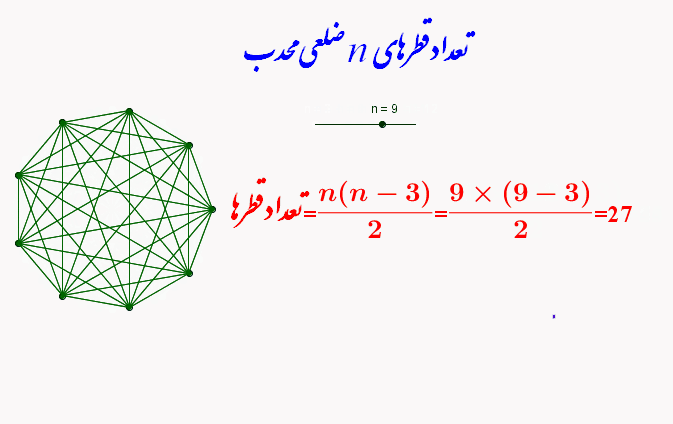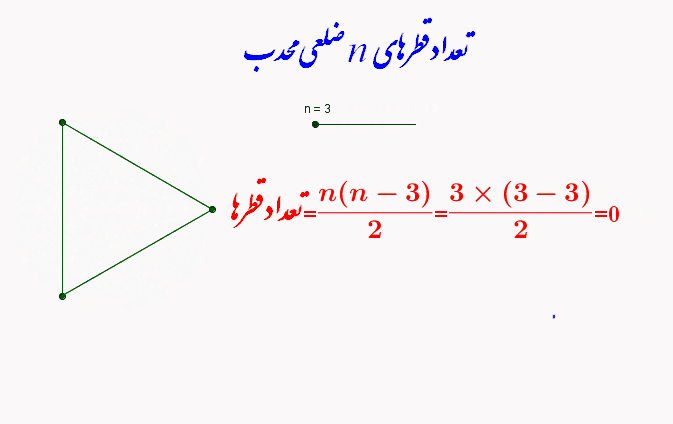
تعداد قطرهای هر چند ضلعی محدب
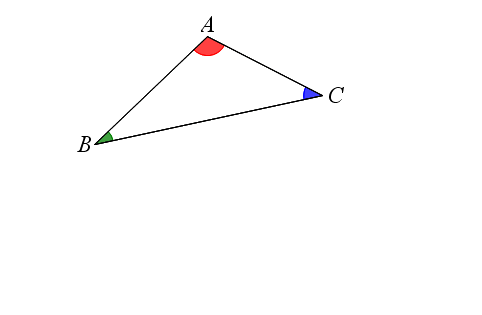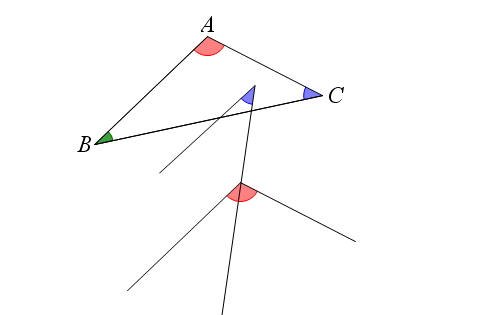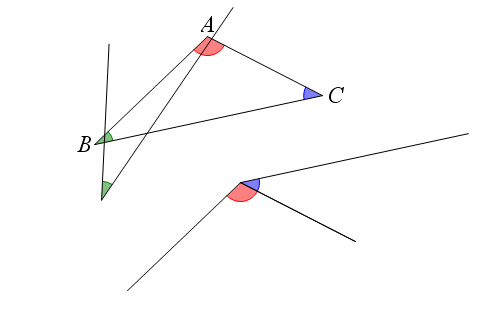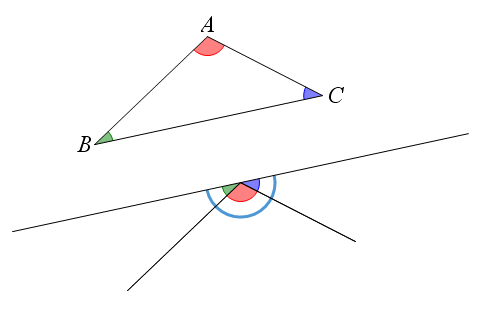
آموزش تصویری مجموع زوایای هر مثلث
فرمولهای بخش اول فصل3 ریاضی هشتم

واکنش های گرماده و گرماگیر
در این مطلب سعی بر آن است تا با تکیه بر مباحث سرعت واکنش و انرژی فعالسازی، واکنش های گرماده و گرماگیر با ارائه نمودار توضیح داده شوند.
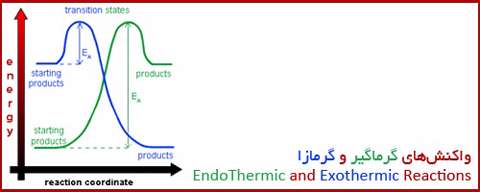
واکنش های گرماده:
طبق نمودار در واکنش های گرماده آنتالپی واکنش دهنده ها (H1) از آنتالپی فراورده ها (H2) بالاتر بوده و گرما آزاد می شود. پیرو مطلب مربوط به نظریه حالت گذار انرژی لازم برای تبدیل واکنش دهنده ها به پیچیده فعال را انرژی فعال سازی واکنش رفت (Ea) و انرژی لازم برای تبدیل فراورده ها به پیچیده فعال را انرژی فعال سازی واکنش برگشت (E'a ) می گویند. در واکنش های گرماده انرژی فعالسازی واکنش رفت کمتر از انرژی فعالسازی واکنش برگشت است؛ در نتیجه سرعت واکنش رفت بیش تر از سرعت واکنش برگشت است. همچنین ∆HD1 یعنی مجموع انرژی پیوندهای مواد واکنش دهنده که برای تبدیل آن ها به رادیکال های تک اتمی لازم است از ∆HD2 ، مجموع انرژی پیوندهای فراورده ها، کمتر است .
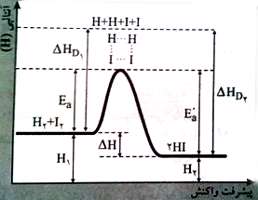
واکنش های گرماگیر:
طبق نمودار در واکنش های گرماگیر آنتالپی واکنش دهنده ها (H1) پایین تر از آنتالپی فراورده ها (H2) است و گرما در طی واکنش مصرف می شود. انرژی فعالسازی واکنش رفت (Ea) در مقایسه با انرژی فعالسازی واکنش برگشت (E'a) بیشتر بوده که این امر باعث می شود در واکنش های گرماگیر سرعت واکنش های رفت کمتر از سرعت واکنش های برگشت باشد. مجموع انرژی پیوندهای مواد واکنش دهنده (∆HD1 ) از مجموع انرژی پیوندهای فراورده ها (∆HD2 ) بیشتر است.
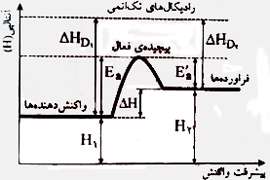
محاسبه آنتالپی ∆H) ) واکنش:
مقادیر H1 و H2 به طور صد در صد قابل محاسبه نیست. در نتیجه درست نیست که برای محاسبه∆H از رابطه
∆H =H2-H1 استفاده کنیم. همان طور که در نمودارهای بالا ملاحظه می کنید، ∆H برابر با اختلافH1 و H2 ، اختلاف
∆HD1 و ∆HD2 ، اختلاف Ea و E'a است. بنابراین طبق این تحلیل و بر اساس کتاب درسی شیمی پیش دانشگاهی برای محاسبه ∆H واکنش می توان از این رابطه استفاده کرد: ∆H =Ea-E'a
بدیهی است مقدار ∆H در واکنش های گرماده منفی و در واکنش های گرماگیر مثبت است.
∆H برگشت:
اگر ∆H واکنش برگشت را از ما بخواهند کافیست ∆H واکنش رفت را محاسبه کنیم و سپس آن را در یک منفی ضرب کنیم. در زیر واکنش های گرماده و گرماگیر مطرح شده در کتاب درسی لیست شده اند که حفظ آن ها برای داوطلبان کنکور بی فایده نیست:
واکنش های گرماده:
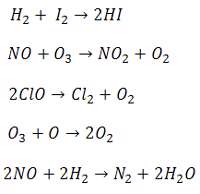
واکنش های گرماگیر:
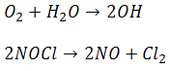
تمرین: در واکنش زیر آنتالپی تشکیل مولی AB چند کیلوژول بر مول است؟
